原来多糖是天然高分子化合物,免疫调节被认为是最重要的生物活性
多糖是一种由10个及以上的单糖聚合而成的天然高分子化合物,广泛存在于动植物中和微生物中,具有多种生物活性,比如调节免疫、抗肿瘤、抗氧化和降血糖等生理功能。
其中,免疫调节作用被认为是其最重要的一种生物活性。
研究人员从组织器官水平、细胞水平、分子水平以及肠道菌群出发,深入研究多糖免疫调节作用及其机制,证明了多糖免疫调节作用并非单一环节,而是多环节、多靶点调节机体的免疫功能。
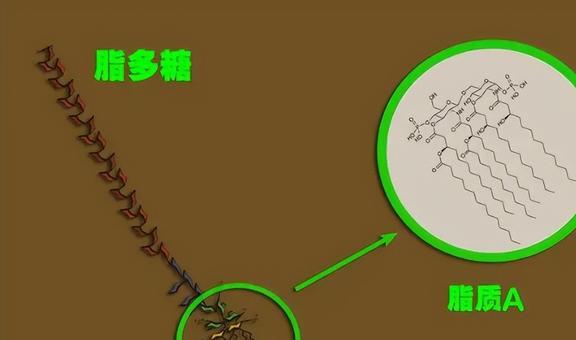
相比多糖的药效学研究,其药动学的研究进展较为缓慢。
由于多糖的相对分子质量较大且无荧光基团或紫外吸收,使得多糖的示踪和检测成为难点。
本文对近年来多糖体内药动学研究、免疫调节作用机制研究的技术进行总结,以期为多糖体内过程及其免疫调节机制研究提供一定的技术参考。

口服给予多糖后,部分多糖难以被唾液或胃液中的酶消化。
肠道中寄生着丰富的肠道菌群,以拟杆菌门和厚壁菌门为主,也包括少量放线菌门和变形菌门。
这些肠道微生物能够分泌多糖降解酶降解多糖,可促进机体对多糖的消化和吸收。
此外,小肠肠黏膜表面积较大,富含丰富的小肠绒毛和肠毛细血管,并且存在特殊的转运体,这些结构特征有助于多糖的体内吸收。
因此,多糖主要是通过肠道吸收后进入体内并发挥药理活性。
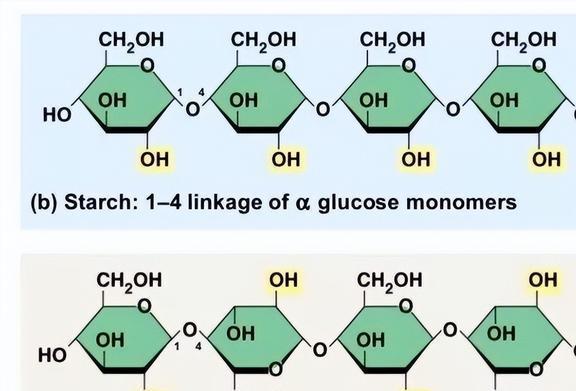
多糖在肠道的吸收方式主要有:细胞旁路通道转运、跨细胞途径和M细胞介导的转运。
多糖通过细胞旁路吸收是一个被动转运的过程,并且由肠上皮细胞紧密连接(tightjunction,TJ)控制,肠道不同节段的上皮细胞紧密连接的空隙各不相同,当肠上皮细胞紧密连接完全打开时,大分子量多糖即可吸收。
多糖的跨细胞途径吸收主要指多糖在肠细胞顶膜处通过胞吞作用从肠腔转运至细胞外液。
M细胞在内吞吸收多糖作用中非常活跃,与肠上皮细胞不同,M细胞的顶端膜缺乏正常的微绒毛,呈现出褶状结构。
此外,其基底膜深凹呈囊状,一些肠道相关的淋巴细胞聚集在此处形成派尔集合淋巴结,且M细胞表面含有多种多糖的特异性受体,可识别外源性多糖并运输给派尔集合淋巴结中的淋巴细胞。
因此,M细胞介导的转运途径对多糖的肠道吸收具有十分重要的意义。
随着研究的不断深入,多糖免疫调节机制的研究已经达到分子和受体的水平。
Toll样受体、清道夫受体、补体受体3和Dectin-1等是目前研究发现的主要多糖受体。

多糖通过识别并结合免疫细胞表面的特定受体,激活细胞内下游信号通路,进而促进相关细胞因子的表达,从而启动免疫反应并发挥免疫调节作用。
多糖与Toll样受体结合后,通过激活髓样分化蛋白88(MyD88)来促进核转录因子-κB(NF-κB)和丝裂原活化蛋白激酶(MAPK)分泌促进肿瘤坏死因子-α (TNF-α)、白细胞介素-1β(IL-1β)、白细胞介素-6(IL-6)等促炎细胞因子。
多糖和清道夫受体结合后,激活p38丝裂原活化蛋白激酶(MAPKp38)及NF-κB两条信号通路,继而促进TNF-α和白细胞介素-12(IL-12)的分泌。
补体受体3(CR3)能识别β-葡聚糖,与白细胞分化抗原14(CD14)形成复合体,共同激活磷脂酶(PLC),继而激活蛋白激酶(PKC)和磷脂酰肌醇-3-激酶(PI3-K),通过MAPK或NF-κB信号通路调控相关细胞因子的表达。
Dectin-1与β-葡聚糖特异性结合后,激活细胞内酪氨酸激酶(Syk),进而激活MAPK或NF-κB信号通路并释放细胞因子。
此外,dectin-1能增强Toll样受体介导的NF-κB信号通路,共同发挥作用,引起免疫应答。
正常情况下,肠道菌群与机体免疫调节系统处于动态平衡状态,维持着肠道微生态的稳定。
多糖进入肠道后与肠道菌群发生相互作用,这些微生物群介导的生物转化将大分子多糖降解为低聚糖或单糖,同时,多糖也能够调节肠道菌群相对丰度,多糖被分解后作用于肠系膜淋巴系统、派尔集合淋巴结以及肠上皮内淋巴细胞,从而下调TGF-β、干扰素-γ (INF-γ)、IL-1β和IL-6等炎症因子来减轻炎症反应。
多糖的免疫调节活性与肠道菌群的作用密切相关。
多糖进入肠道后在肠道菌群的作用下降解为单糖或低聚糖,经代谢最终生成一系列短链脂肪酸(SCFAs)。
而SCFAs对调控宿主免疫具有重要作用。
SCFAs主要通过激活免疫细胞趋化、分化、增殖和凋亡来参与机体免疫调控,这些调控过程主要通过激活G蛋白偶联受体(GPCRs)和抑制组蛋白去乙酰化酶(HDAC)活性来实现。

SCFAs与G蛋白偶联受体109a(GPR109a)结合,抑制NF-κB的激活,从而下调TNF-α、白细胞介素-2(IL-2)、IL-6和转化生长因子-β (TGF-β)等炎症因子的表达,GPR109a的激活还可促进Treg细胞的转录因子Foxp3的表达,使得Treg细胞数目增加,从而抑制炎症的发生。
SCFAs通过激活GPR41促进缺氧诱导因子1α (HIF-1α)的表达来上调抗炎因子白细胞介素-22(IL-22)的产生,提高肠道细胞的免疫活性。
G蛋白偶联受体43(GPR43)的激活可促进Th1细胞的分化以及炎性因子白细胞介素-10(IL-10)的释放。
此外,SCFAs可直接通过抑制HDAC活性来调节免疫反应,当HDAC受到抑制后会导致NF-κB失活,从而减少促炎细胞因子的生成。
SCFAs能够刺激肠黏膜中B细胞分泌免疫球蛋白A(IgA),并且其诱导分泌型免疫球蛋白A(sIgA)的释放,维持机体免疫平衡。

多糖能够与细胞膜表面的分子结合形成糖蛋白,进而参与信号传导并发挥免疫调节作用。
然而由于多糖本身无发光基团,导致其难以在复杂体系中定性或定量分析,进而使得多糖在体内的吸收、分布、代谢和消除的相关研究存在相对不足,这在一定程度上限制了多糖药代动力学的深入研究。
目前,多糖体内药动学研究以荧光标记法和同位素标记法较为常用。
荧光标记法是将多糖分子上的活性基团(如羟基、氨基、羧基等)与荧光素以共价偶联的方式进行结合,通过检测荧光强度对多糖进行定性、定量分析。
被标记后的多糖因具有荧光发光基团,可排除内源性多糖物质的干扰。
研究人员通过该技术实现对多糖的吸收、分布、代谢、排泄各环节的监测,有利于多糖药代动力学的深入研究。
Liang等采用荧光素5-异硫氰酸酯(FITC)标记半乳糖基化壳聚糖(GC)的方法研究其在小鼠体内的器官靶向性,结果表明FITC-GC在静脉注射5min后在肝脏显著富集,48h后仍可在肝脏中检测到。
相比之下,FITC-GC在肝脏中比FITC-CS(未加半乳糖修饰的壳聚糖)富集浓度更高。
Kaneo等研究了静脉注射后大鼠血浆中FITC标记的阿拉伯半乳聚糖(FA)的全身分布与消除,研究发现,FA在静脉注射30min后在血浆中被清除,随后主要分布在肝脏和肾脏中。

Zhang等研究了经FITC标记的当归多糖(ASP)静脉给药后的药代动力学信息,研究发现,ASP在静脉注射后能够迅速从血液中消除并以高特异性分布到肝脏,且在体内未发生降解。
荧光标记法不仅可以给多糖定量,还可以确定多糖在体内是否被降解,这是荧光标记法的优点。
然而,荧光标记法在多糖药代动力学研究中仍存在一定的不足,荧光标记后的多糖的敏感性不强,仅能在浓集器官和血液中检测到,因此会增加操作的复杂性。
FITC中的异硫氰酸酯基团与氨基具有高反应性,在一定条件下可直接发生亲核加成反应,因此,FITC被广泛用于多糖的荧光标记。
而羟基对N-甲基靛红酸酐(MIA)的反应基团苯并噁嗪环具有特异性反应,直接以偶联的方式结合。
含糖醛酸的酸性多糖可用含氨基的荧光素ANDSA直接标记,用过量的1-乙基-3-(3-二甲基氨丙基)-碳化二亚胺(EDC)将多糖活化后,直接加入荧光素ANDSA接入发光基团。
因此,不同多糖荧光标记的位置也各不相同,常用的荧光标记位点主要分为三类,

Group
Fluorescein
Polysaccharide
Hydroxylgroupsofpolysaccharides(-OH)
5-DTAF
Konjacmannan,yeastpolysaccharides
FITC
Angelicapolysaccharides,Ganodermalucidumpolysaccharides,Gojiberrypolysaccharides
RBITC
Dendroglossanpolysaccharides,Dextran
MIA
Dextran
Aminogroupsofpolysaccharides(-NH2)
AF
Seaweedpolysaccharides
Aldehydegroupofpolysaccharides(-CHO)
APTS
Malto-oligosaccharides
ANTS
Sulfatephycosan
放射性同位素由于其放射强度和半衰期各不相同,在体内的药物代谢动力学研究会呈现不同的特点。
为了解决多糖体内检测技术的局限带来的一系列难题,放射性同位素标记技术也开始运用到多糖的代谢动力学研究中,由于放射性同位素能够自发地发射特征谱线,在体外与多糖分子结合后可以利用核探测器、电子计算机断层扫描(computedtomography,CT)对多糖进行定量、定位检测,用于追踪多糖在体内发挥免疫调节作用的代谢途径。
常用的放射性同位素有:14C、3H、125I、99mTc等。















